Gas oksigen (O2) adalah salah satu elemen penting yang digunakan dalam berbagai aplikasi, baik di industri maupun di laboratorium. Di laboratorium, gas oksigen sering digunakan dalam eksperimen kimia, penelitian biologi, dan proses pembakaran. Pembuatan gas oksigen di laboratorium dapat dilakukan dengan beberapa cara yang efisien dan aman. Artikel ini akan menjelaskan secara rinci proses dan metode pembuatan gas oksigen di laboratorium.
1. Dekomposisi Hidrogen Peroksida (H2O2)
Salah satu metode yang umum digunakan untuk memproduksi gas oksigen di laboratorium adalah melalui dekomposisi hidrogen peroksida (H2O2). Hidrogen peroksida adalah senyawa kimia yang mengandung dua atom hidrogen dan dua atom oksigen. Ketika hidrogen peroksida didekomposisi, gas oksigen dilepaskan.
Proses dekomposisi dapat dilakukan dengan menggunakan katalisator seperti besi(III) oksida (Fe2O3) atau kalium permanganat (KMnO4). Hidrogen peroksida ditambahkan ke dalam labu reaksi bersama dengan katalisator, dan kemudian dipanaskan. Reaksi dekomposisi menghasilkan gas oksigen dan air.
Keuntungan menggunakan metode dekomposisi hidrogen peroksida adalah bahwa reaksinya relatif cepat dan sederhana. Namun, perlu diingat bahwa hidrogen peroksida adalah bahan yang mudah terbakar dan berpotensi berbahaya. Oleh karena itu, perlu dilakukan dengan hati-hati dan di bawah pengawasan yang tepat.
2. Elektrolisis Air
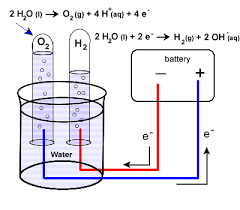
Metode lain yang populer untuk pembuatan gas oksigen di laboratorium adalah elektrolisis air. Elektrolisis air melibatkan penggunaan arus listrik untuk memisahkan molekul air (H2O) menjadi gas oksigen (O2) dan hidrogen (H2).
Proses elektrolisis dilakukan dengan menggunakan sel elektrolisis, yang terdiri dari dua elektroda, yaitu katoda dan anoda, yang terendam dalam larutan elektrolit seperti natrium sulfat (Na2SO4). Arus listrik dialirkan melalui larutan elektrolit, dan pada katoda terbentuk gas hidrogen, sedangkan pada anoda terbentuk gas oksigen.
Kelebihan metode elektrolisis air adalah bahwa sumber bahan baku yang digunakan, yaitu air, mudah didapatkan dan aman. Namun, perlu diperhatikan bahwa elektrolisis air membutuhkan pasokan listrik yang stabil dan efisien, serta peralatan elektrolisis yang sesuai.
3. Penggunaan Zat Pemutih
Metode lain yang dapat digunakan untuk menghasilkan gas oksigen di laboratorium adalah dengan menggunakan zat pemutih yang mengandung senyawa oksigen. Salah satu contoh zat pemutih yang sering digunakan adalah hidrogen peroksida yang terkandung dalam zat pemutih rumah tangga.
Proses ini melibatkan penambahan zat pemutih ke dalam larutan asam, seperti asam sulfat (H2SO4). Reaksi antara zat pemutih dan asam menghasilkan gas oksigen. Namun, perlu diingat bahwa penggunaan zat pemutih rumah tangga sebagai sumber gas oksigen mungkin tidak seefisien atau seaman metode lain yang telah disebutkan sebelumnya.
Kesimpulan
Pembuatan gas oksigen di laboratorium dapat dilakukan dengan beberapa cara yang telah dijelaskan di atas. Metode dekomposisi hidrogen peroksida, elektrolisis air, dan penggunaan zat pemutih adalah beberapa metode yang umum digunakan. Pemilihan metode tergantung pada faktor-faktor seperti kecepatan reaksi, ketersediaan bahan baku, dan keamanan. Penting untuk selalu memperhatikan protokol keamanan dan menggunakan peralatan yang sesuai saat melakukan proses pembuatan gas oksigen di laboratorium.
Dengan pemahaman yang baik tentang proses dan metode ini, laboratorium dapat memproduksi gas oksigen dengan efisien dan aman untuk memenuhi kebutuhan eksperimen dan penelitian mereka.
 Spirit Kawanua News Portal Berita Terbaik di Sulawesi Utara Yang Menyajikan Beragam Berita Teraktual, Terpercaya dan Terbaru.
Spirit Kawanua News Portal Berita Terbaik di Sulawesi Utara Yang Menyajikan Beragam Berita Teraktual, Terpercaya dan Terbaru.